VnHocTap.com trình làng cho tới những em học viên lớp 10 nội dung bài viết Viết công thức electron, công thức cấu trúc của phân tử, nhằm mục đích chung những em học tập đảm bảo chất lượng lịch trình Hóa học tập 10.
Bạn đang xem: công thức electron

Xem thêm: Nạp tiền Mu88: Hướng dẫn và các phương thức nhanh chóng

Xem thêm: dđinh lăng


Nội dung nội dung bài viết Viết công thức electron, công thức cấu trúc của phân tử:
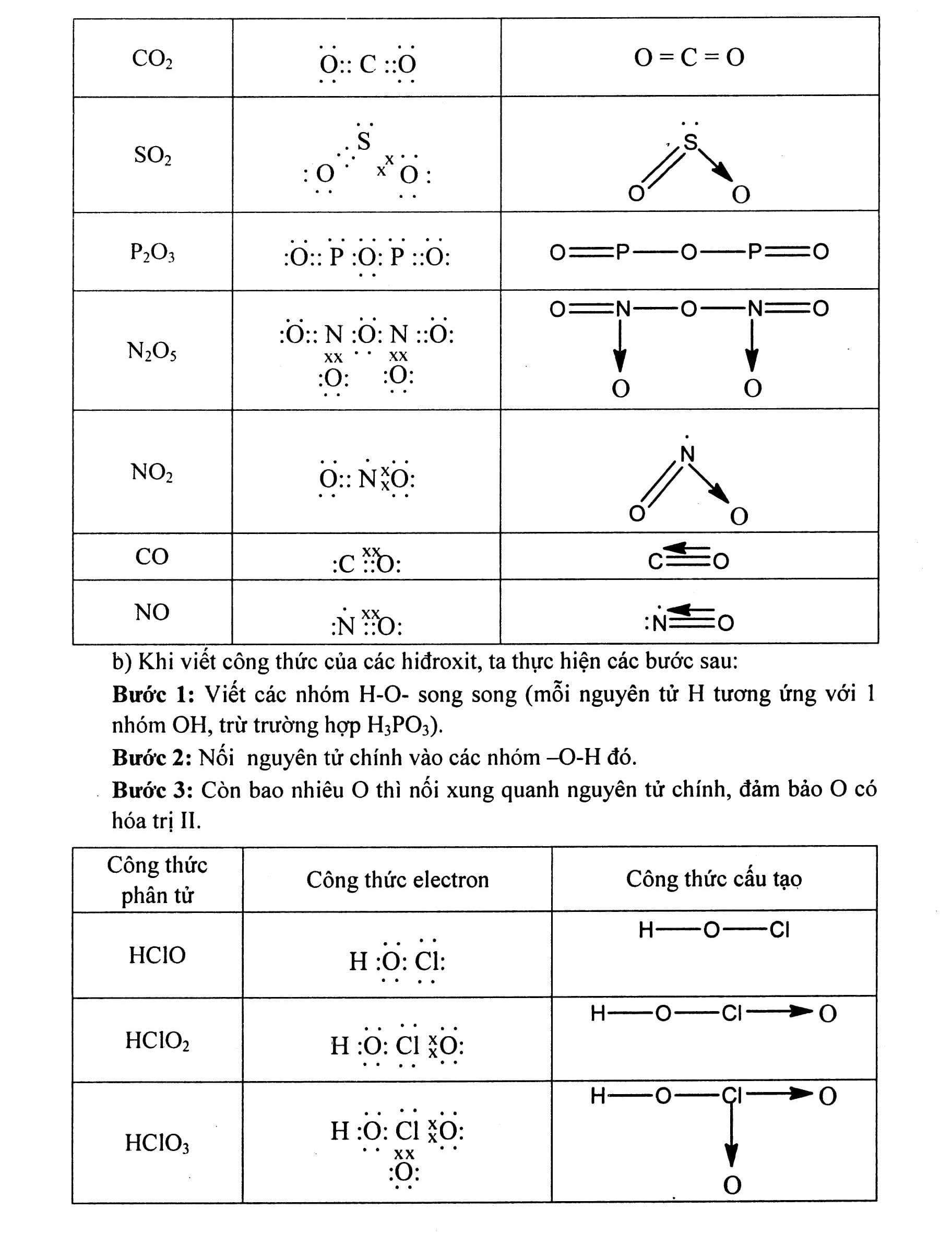
Công thức electron màn biểu diễn vì chưng những lốt chấm. Công thức cấu trúc màn biểu diễn vì chưng những lốt gạch ốp nối. Mẹo: Khi ghi chép công thức electron và công thức cấu trúc nên ghi chép công thức cấu trúc trước phụ thuộc vào hóa trị của những yếu tắc tiếp tục biết tiếp sau đó mã hóa trở thành công thức electron bằng phương pháp thay cho từng lốt gạch ốp nối ứng vì chưng 2 lốt chấm. Tuy nhiên công thức electron hoàn toàn có thể màn biểu diễn theo đuổi qui tắc chén bát tử (xung xung quanh từng nguyên vẹn tử đều phải sở hữu 8e). Khi ghi chép theo phong cách này thì cấu trúc thông thường chứa chấp tăng link mang lại – nhận.
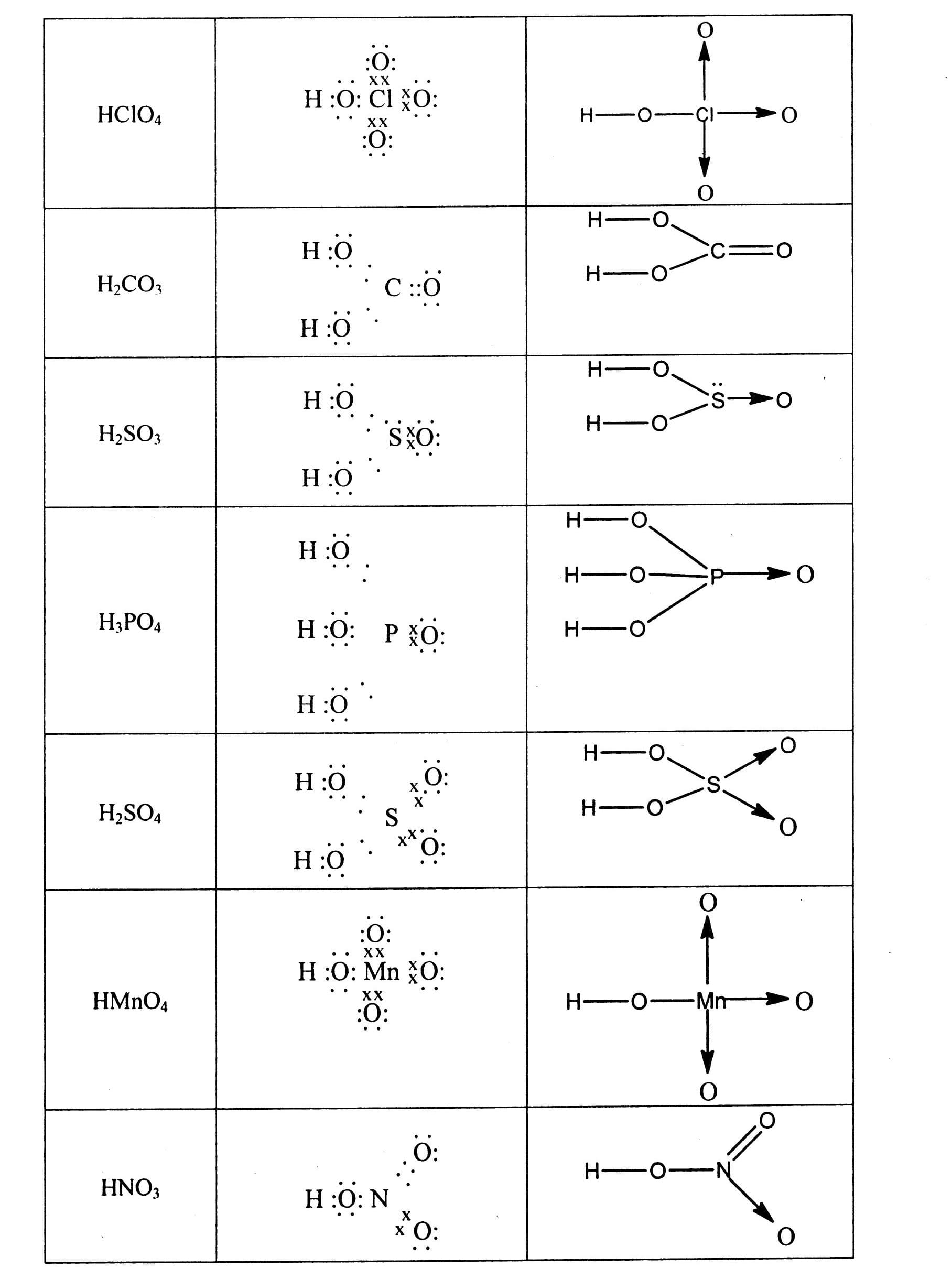
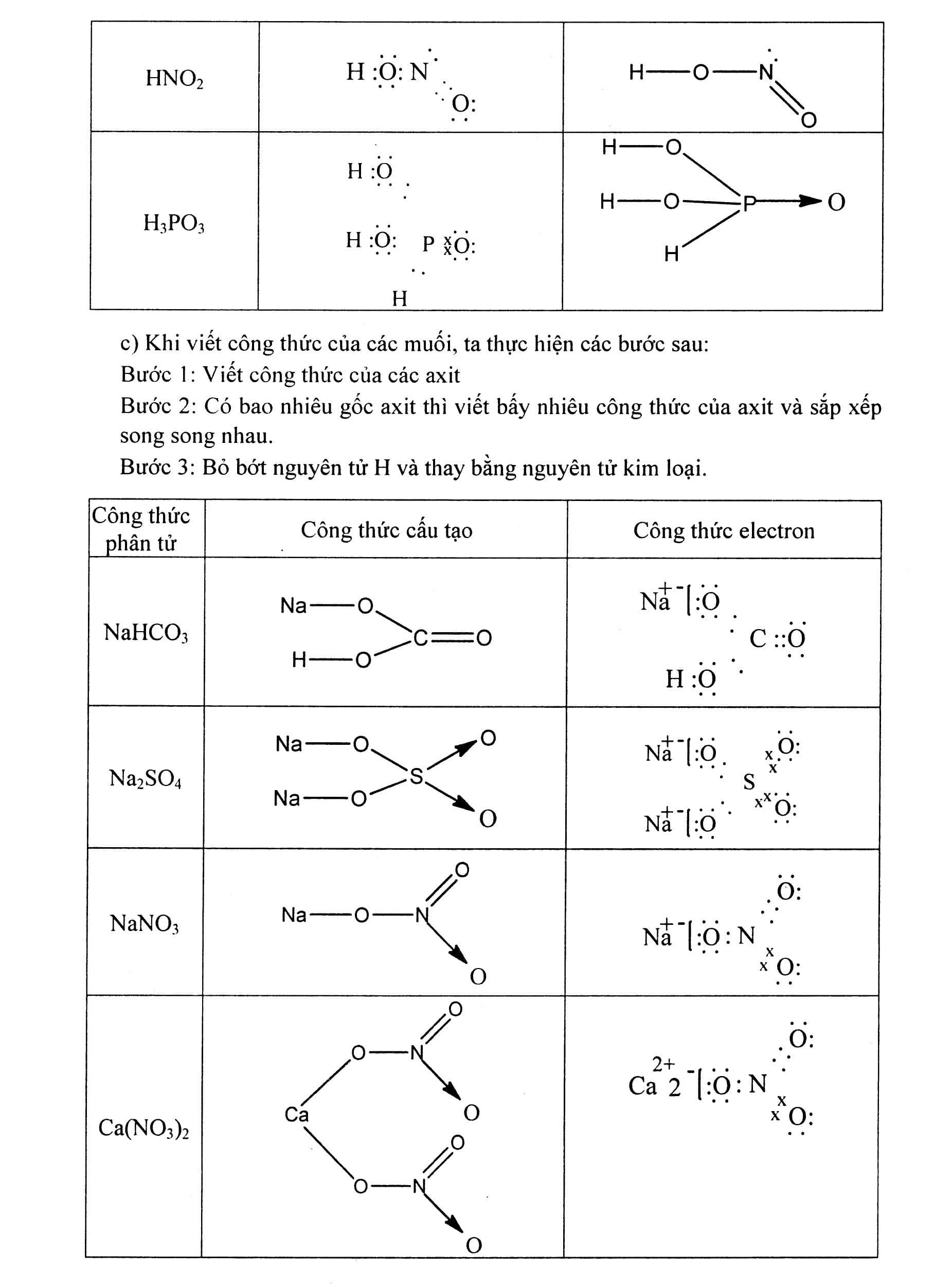
Bài 1: Viết công thức cấu trúc và công thức electron của những phân tử sau: N2, NH3, CH4, C2H4, C2H2, Cl2, HCl, H2O, H2S. Hướng dẫn giải Công thức phân tử Công thức electron Công thức cấu trúc. Bài 2: Viết công thức electron và công thức cấu trúc của những phân tử Hướng dẫn giải a) Khi ghi chép công thức của những oxit dạng R2Ox, tao triển khai công việc sau: Cách 1: Viết một nguyên vẹn tử O trước. Cách 2: Nối nhì nguyên vẹn tử chủ yếu nhập nguyên vẹn tử O cơ. Cách 3: Còn từng nào O thì chia đều cho các bên và nối xung xung quanh nhì nguyên vẹn tử chủ yếu, đáp ứng O sở hữu hóa trị II. b) Khi ghi chép công thức của những hiđroxit, tao triển khai công việc sau: Cách 1: Viết những group H-O- tuy nhiên song (mỗi nguyên vẹn tử H ứng với cùng 1 group OH, trừ tình huống H3PO3). Cách 2: Nối nguyên vẹn tử chủ yếu nhập những group -O-H cơ. Cách 3: Còn từng nào O thì nối xung xung quanh nguyên vẹn tử chủ yếu, đáp ứng O sở hữu hóa trị II. Công thức phân tử Công thức electron Công thức cấu trúc c) Khi ghi chép công thức của những muối hạt, tao triển khai công việc sau: Cách 1: Viết công thức của những axit Cách 2: Có từng nào gốc axit thì ghi chép từng ấy công thức của axit và bố trí tuy nhiên song nhau. Cách 3: Bỏ hạn chế nguyên vẹn tử H và thay cho vì chưng nguyên vẹn tử sắt kẽm kim loại.
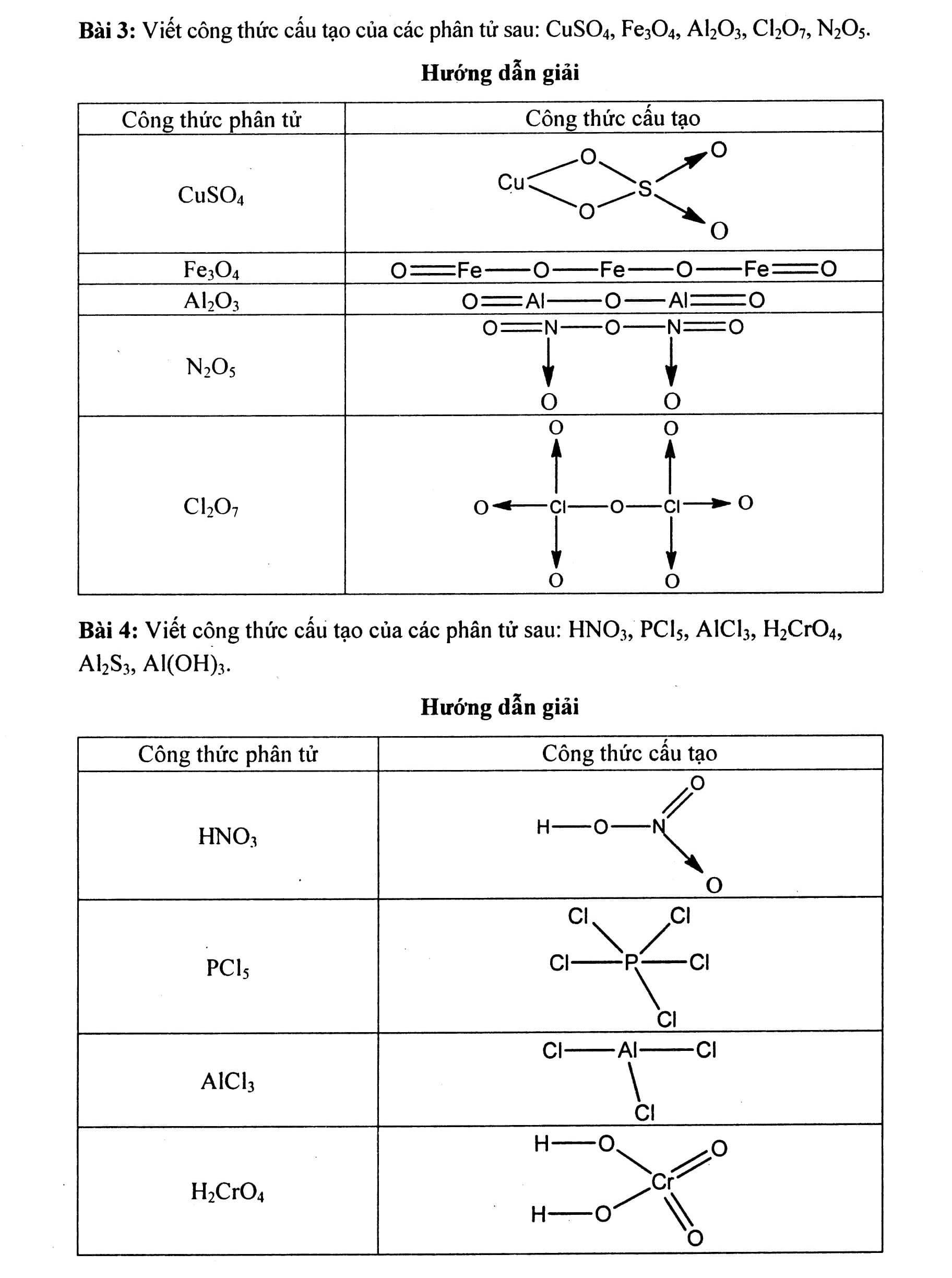
Bài 3: Viết công thức cấu trúc của những phân tử sau: CuSO4, Fe3O4, Al2O3, Cl2O7, N2O5. Bài 4: Viết công thức cấu trúc của những phân tử sau: HNO3, PCl5, AlCl3, H2CrO4, Al2S3, Al(OH)3. Bài 5: Viết công thức cấu trúc và công thức electron của BF3 và NH3. Giải mến vì sao BF3 hoàn toàn có thể phối kết hợp được với NH3. Hướng dẫn giải Trong phân tử BF3 nguyên vẹn tử B xung xung quanh mới nhất sở hữu 6e, vẫn còn đó thiếu hụt 2e mới nhất đạt thông số kỹ thuật 8e lớp bên ngoài nằm trong vững chắc. Trong phân tử NH4, nguyên vẹn tử N sở hữu một cặp electron tự tại ko link. Cặp electron tự tại này sẽ khởi tạo link mang lại – nhận với nguyên vẹn tử B nhập BF3 Bài 6: Viết công thức cấu trúc và công thức electron của CO2 và SO2. Giải mến vì sao SO2 hoàn toàn có thể kết phù hợp với oxi tạo nên trở thành SO3 còn CO2 không tồn tại kỹ năng cơ. Hướng dẫn giải: Trong phân tử SO2, nguyên vẹn tử S còn một cặp electron ko link, sở hữu kỹ năng tạo nên link mang lại – nhận với cùng 1 nguyên vẹn tử oxi (còn thiếu hụt chính 2e nhằm đạt thông số kỹ thuật 8e lớp bên ngoài cùng). Còn nhập phân tử CO2, nguyên vẹn tử C không hề electron tự tại và đã và đang đạt thông số kỹ thuật 8e lớp bên ngoài nằm trong vững chắc nên nó không tồn tại kỹ năng kết phù hợp với oxi được nữa.













Bình luận